En el contexto de la aceleración continua de la innovación farmacéutica global, los medicamentos huérfanos (Orphan Drugs) están pasando de ser un “campo marginal” a convertirse en una “pista central”. Con la mejora de las políticas regulatorias de incentivo, los avances en medicina de precisión y el aumento sostenido de la inversión, el desarrollo de fármacos para enfermedades raras ha entrado en una fase de aceleración. Especialmente alrededor de 2026, un grupo representativo de 5 terapias innovadoras clave se encuentra en etapas clínicas críticas y ha demostrado el potencial de transformar el panorama terapéutico.
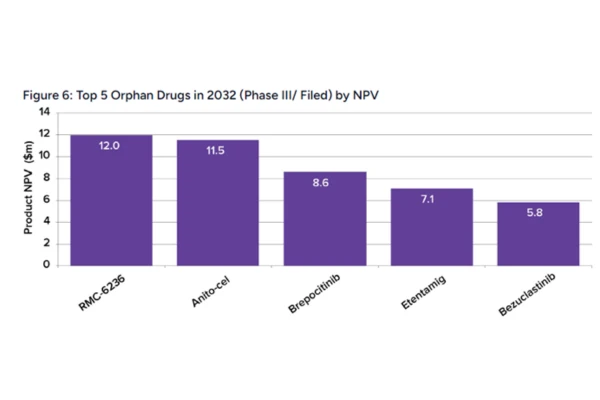
A diferencia del modelo tradicional centrado en el “tratamiento sintomático”, esta nueva ola de innovación en medicamentos huérfanos pone mayor énfasis en el “mecanismo de acción” y la “intervención precisa”. Desde fármacos dirigidos de molécula pequeña hasta terapias celulares CAR-T, desde anticuerpos biespecíficos hasta inhibidores multiblanco de vías de señalización, múltiples enfoques tecnológicos están remodelando el tratamiento de las enfermedades raras. Dengyue Pharma se centra en cinco terapias candidatas representativas, analizando cómo impulsan la evolución de los paradigmas terapéuticos en diferentes áreas de enfermedad.
Inhibidor de RAS Daraxonrasib: abordando el “objetivo difícil” del cáncer de páncreas
La vía RAS ha sido considerada durante mucho tiempo uno de los objetivos más desafiantes en el tratamiento del cáncer, especialmente en el cáncer de páncreas, donde la tasa de mutación de KRAS es extremadamente alta, pero históricamente ha carecido de terapias dirigidas eficaces. Como representante clave dentro de las 5 terapias innovadoras clave, la aparición de Daraxonrasib se considera un avance significativo en este campo.
Este fármaco actúa interviniendo directa o indirectamente en nodos críticos de la vía de señalización RAS, inhibiendo la proliferación y supervivencia de las células tumorales. A diferencia de los inhibidores tradicionales de KRAS G12C, Daraxonrasib enfatiza una mayor cobertura de múltiples subtipos de mutaciones RAS, ampliando así la población potencialmente beneficiada. Sus principales ventajas incluyen:
- Mayor cobertura de mutaciones RAS
- Inhibición sostenida de vías de señalización downstream
- Buen potencial de combinación con otras terapias
En una indicación con pronóstico tan desfavorable como el cáncer de páncreas, cualquier avance sustancial tiene gran relevancia. Daraxonrasib no solo representa una mejora en la “accesibilidad del objetivo”, sino que también indica que la terapia dirigida a RAS está evolucionando de avances puntuales hacia un control sistémico.
Evolución de CAR-T: Anitocabtagene autoleucel logra equilibrio entre eficacia y seguridad
La terapia CAR-T ha demostrado un éxito notable en neoplasias hematológicas, pero los problemas de seguridad, como el síndrome de liberación de citocinas (CRS) y la neurotoxicidad, siguen limitando su aplicación generalizada. Anitocabtagene autoleucel (anito-cel) representa una optimización bajo este contexto.
Mediante mejoras en el diseño estructural del CAR y el control de la expansión celular, esta terapia mantiene una alta actividad antitumoral al tiempo que reduce eventos adversos graves. Sus mecanismos incluyen:
- Reconocimiento preciso de antígenos tumorales
- Control de la expansión in vivo de células CAR-T
- Reducción de la toxicidad por hiperactivación inmune
Desde la perspectiva de las 5 terapias innovadoras clave, la terapia celular está evolucionando de “alta potencia” a “precisión controlable”, convirtiéndose en una herramienta terapéutica personalizada.
Doble inhibición TYK2/JAK1: Brepocitinib explora nuevas vías en dermatomiositis
La dermatomiositis, como enfermedad autoinmune rara, ha enfrentado durante mucho tiempo la falta de opciones terapéuticas eficaces. Brepocitinib, mediante la inhibición dual de TYK2 y JAK1, regula la inflamación desde su origen.
Sus mecanismos incluyen:
- Inhibición de múltiples vías de citocinas inflamatorias
- Reducción de la activación inmune anormal
- Mejora del daño inflamatorio muscular y cutáneo
En el marco de las 5 terapias innovadoras clave, este enfoque impulsa la transición del tratamiento sintomático hacia la intervención basada en mecanismos.
Anticuerpos biespecíficos: Etentamig redefine el tratamiento del mieloma múltiple
El mieloma múltiple (MM) presenta necesidades no cubiertas significativas en etapas de recaída o refractariedad. Etentamig, como representante de anticuerpos dentro de las 5 terapias innovadoras clave, actúa conectando células tumorales con células inmunes para inducir una citotoxicidad directa.
Su mecanismo incluye:
- Reconocimiento del antígeno tumoral
- Activación de células T
- Inducción de destrucción tumoral
Su ventaja radica en no requerir modificación celular, lo que le confiere mayor accesibilidad en comparación con CAR-T.
Mutaciones KIT: Bezuclastinib amplía el tratamiento de GIST y mastocitosis sistémica
Las mutaciones en KIT desempeñan un papel clave en GIST y mastocitosis sistémica (SM), pero la resistencia limita la eficacia de los tratamientos actuales. Bezuclastinib aborda este desafío mediante una estrategia de “doble canal”.
Sus ventajas incluyen:
- Inhibición de mutaciones resistentes
- Alta selectividad
- Cobertura de múltiples indicaciones
Las 5 terapias innovadoras clave están evolucionando desde el enfoque de “una enfermedad” hacia terapias basadas en mecanismos compartidos.
Tendencias detrás de las 5 terapias innovadoras clave
- De control sintomático a intervención mecanística
- Desarrollo paralelo de múltiples tecnologías
- Medicina de precisión como eje central
- Terapias combinadas como estándar emergente
Perspectiva futura: aceleración hacia la aplicación clínica
Con el avance de Daraxonrasib, anito-cel, brepocitinib, etentamig y bezuclastinib, el tratamiento de enfermedades raras está evolucionando de “sin opciones terapéuticas” a “intervención precisa”.
En los próximos años, con la publicación de más datos de fase III y la aprobación de nuevos fármacos, los pacientes tendrán más opciones terapéuticas. Al mismo tiempo, la mejora de las cadenas globales de suministro farmacéutico y los sistemas de acceso transfronterizo facilitará la disponibilidad de terapias innovadoras. En este proceso, plataformas como Hong Kong Dengyue Pharma están promoviendo el acceso eficiente a medicamentos huérfanos mediante redes globales y suministro conforme a normativa.
Se prevé que el tratamiento de enfermedades raras alcance un punto de inflexión: de “retrasar la progresión” a “modificar la historia natural de la enfermedad”, y de avances aislados a innovación sistemática. El año 2026 podría marcar el inicio real de esta transformación.

FAQ About 5 terapias innovadoras clave
Son cinco enfoques terapéuticos avanzados que incluyen fármacos dirigidos, terapias celulares como CAR-T, anticuerpos biespecíficos y moduladores de vías de señalización, diseñados para tratar enfermedades raras mediante mecanismos precisos.
Porque representan un cambio de paradigma: pasan del control de síntomas a la intervención basada en mecanismos, con el potencial de modificar la progresión de la enfermedad y mejorar significativamente los resultados clínicos.
Incluyen múltiples plataformas como:
·Terapias dirigidas de molécula pequeña
·Terapias celulares CAR-T
·Anticuerpos biespecíficos
·Inhibidores multiblanco (como TYK2/JAK1)
Principalmente enfermedades raras y algunos cánceres difíciles de tratar, como cáncer de páncreas, mieloma múltiple, dermatomiositis, GIST y mastocitosis sistémica.

