En el campo del tratamiento de la hepatitis B, el GST-HG131, el primer inhibidor oral de molécula pequeña del antígeno de superficie de la hepatitis B desarrollado por Guang Sheng Tang Pharmaceutical, ha logrado recientemente avances significativos.
Los datos de su ensayo clínico de fase II se incluyeron en la sección de «Resumen de los últimos avances» de la Reunión Anual 2025 de la Asociación Americana para el Estudio de las Enfermedades Hepáticas (AASLD) y se presentarán allí mismo, lo que demuestra el alto reconocimiento de este innovador logro por parte de la comunidad académica internacional.
👍Este avance ofrece una solución completamente nueva al desafío global de lograr la cura clínica de la hepatitis B.

Innovación de mecanismos: Dirigirse a la secreción de HBsAg para reiniciar la respuesta inmunitaria
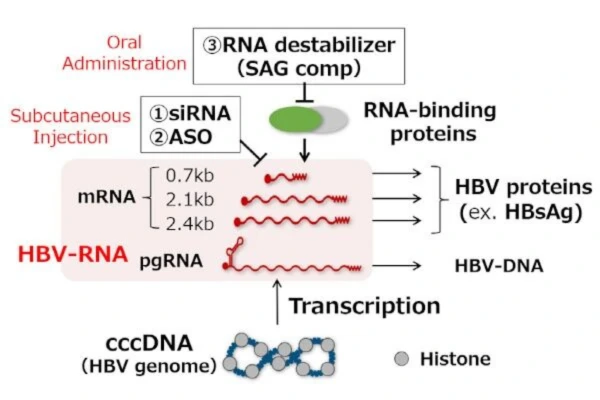
GST-HG131 inhibe la polimerización de la cola poli(A) del ARN del VHB, acelerando la degradación del ARN viral y, por lo tanto, bloqueando la síntesis del antígeno de superficie de la hepatitis B (HBsAg).
Un nivel sostenido de HBsAg inferior a 100 UI/ml se considera un umbral clave para lograr la curación clínica de la hepatitis B. Este nivel mejora significativamente el pronóstico a largo plazo del paciente, reduce el riesgo de cirrosis y cáncer de hígado, y aumenta la sensibilidad del organismo a la inmunoterapia.
A diferencia de los análogos de nucleósidos existentes que solo inhiben la replicación viral, GST-HG131 actúa directamente sobre la secreción de HBsAg, creando las condiciones necesarias para que el sistema inmunitario elimine el virus.
Datos de la fase II: Reducción rápida y profunda del HBsAg, el 76,5% de los pacientes alcanzaron los niveles objetivo
En el ensayo clínico de fase II, GST-HG131 demostró una eficacia significativa:
- Inicio de acción rápido: Algunos pacientes experimentaron una disminución en los niveles de HBsAg de aproximadamente 0,8 log10 UI/ml a los 7 días de tratamiento;
- Reducción profunda: En el grupo de dosis de 30 mg (dos veces al día durante 12 semanas), la reducción promedio de HBsAg fue del 87,12 %, con una reducción máxima del 97,71 %;
- Tasa de consecución del objetivo clave: El 76,5 % de los pacientes alcanzó niveles de HBsAg ≤100 UI/ml, sentando las bases para la terapia combinada posterior para lograr la curación clínica;
- Rebote controlable tras la interrupción: El rebote de HBsAg tras la interrupción fue significativamente menor que el basal, lo que sugiere que el fármaco tiene un efecto duradero.
Terapia combinada: Un régimen totalmente oral desafía la «cura clínica» de la hepatitis B
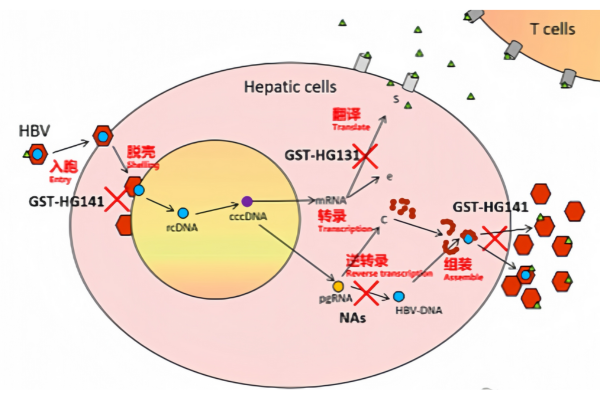
El «Plan Cumbre para la Cura Clínica de la Hepatitis B» de Guangshengtang se centra en el uso combinado de GST-HG131 y otro fármaco en investigación, GST-HG141.
GST-HG141, como inhibidor de la nucleocápside, inhibe eficazmente la replicación viral y reduce el ADN circular cerrado covalentemente (CCCDNA), mientras que GST-HG131 reactiva la respuesta inmunitaria al disminuir los niveles de HBsAg.
Este mecanismo de «inhibición de doble vía» genera un efecto sinérgico y se ha incluido en el «Proyecto Piloto Nacional para la Optimización de la Revisión y Aprobación de Ensayos Clínicos de Fármacos Innovadores».
El régimen totalmente oral mejora significativamente el acceso y la adherencia del paciente, lo que lo hace adecuado para un mayor número de pacientes.
Reconocimiento internacional y perspectivas de industrialización
Tras la presentación de los datos de la fase II de GST-HG131 en la Reunión Anual de la AASLD, el fármaco captó la atención de la comunidad hepatológica mundial y atrajo a numerosas compañías farmacéuticas multinacionales interesadas en colaborar.
En julio de 2025, la Administración Nacional de Productos Médicos de China (NMPA) incluyó el fármaco en su lista de «Terapias Innovadoras», y posteriormente se llevará a cabo un ensayo clínico confirmatorio de fase III.
Si se lanza con éxito, se espera que GST-HG131 cubra la necesidad mundial de medicamentos orales para la hepatitis B, ofreciendo una opción de tratamiento eficaz a casi 300 millones de pacientes con hepatitis B, con un mercado potencial superior a los 100 mil millones de yuanes.

Conclusión
El desarrollo revolucionario de GST-HG131 marca la entrada de las empresas farmacéuticas chinas innovadoras al liderazgo mundial en el tratamiento de la hepatitis B.
Desde el descubrimiento de la diana terapéutica hasta la validación clínica, la trayectoria de I+D de Guang Sheng Tang demuestra una vía eficaz para trasladar la investigación básica a la práctica clínica.
Dengyue Pharma cree con el avance de los ensayos clínicos de fase III, se espera que este fármaco «Hecho en China» transforme el panorama del tratamiento de la hepatitis B, convirtiendo la «cura clínica» de una visión a una realidad.

FAQ About GST-HG131:
Según la información actual, se prevé que el innovador fármaco GST-HG141 de Guang Sheng Tang para el tratamiento de la hepatitis B reciba la aprobación para su comercialización a partir del cuarto trimestre de 2026.
1. Previsión de precios en el mercado nacional: Si la terapia combinada con GST-HG141 está cubierta por el seguro médico, se estima que el precio de un tratamiento (6 meses) oscilará entre 5.000 y 8.000 RMB. Si no está cubierta, el precio podría alcanzar entre 12.000 y 20.000 RMB por tratamiento.
2. Precios de referencia en el mercado internacional: Tomando como referencia los precios internacionales de otros medicamentos y considerando la asequibilidad en los países en desarrollo, el precio estimado de GST-HG141 en los mercados extranjeros podría oscilar entre 10.000 y 30.000 USD por tratamiento.
GST-HG141 ha demostrado una actividad antiviral significativa y un buen perfil de seguridad en un ensayo clínico de fase II, lo que proporciona una base sólida para su entrada en un ensayo clínico confirmatorio de fase III.
Entecavir y tenofovir

