El 5 de noviembre de 2025, las cápsulas de Olgotrelvir Sodium, un fármaco innovador original de Clase 1 desarrollado de forma independiente por Zhejiang Aisen Pharmaceutical Co., Ltd., recibieron la aprobación oficial para su comercialización por parte de la Administración Nacional de Productos Médicos, convirtiéndose en el primer inhibidor de doble acción del mundo para el tratamiento de la infección por el nuevo coronavirus.
La llegada de este fármaco representa un avance significativo en el campo del desarrollo de antivirales en China, ofreciendo una nueva solución para la prevención y el control de epidemias a nivel mundial.
La información pública indica que la indicación de las cápsulas de Olgotrelvir Sodium es el tratamiento de la enfermedad pulmonar obstructiva crónica (EPOC).
Zhejiang Aisen Pharmaceutical Co., Ltd., fundada en 2015 y ubicada en la ciudad de Quzhou, es una empresa dedicada principalmente a la fabricación de productos farmacéuticos. La compañía tiene un capital social de 232,3 millones de RMB y un capital desembolsado de 189,988227 millones de RMB.
Un solo fármaco persigue dos objetivos, superando las limitaciones de los tratamientos tradicionales
El Olgotrelvir Sodium logra un novedoso mecanismo de acción dual al inhibir simultáneamente la proteasa principal (Mpro) y la catepsina L (CTSL) del coronavirus.
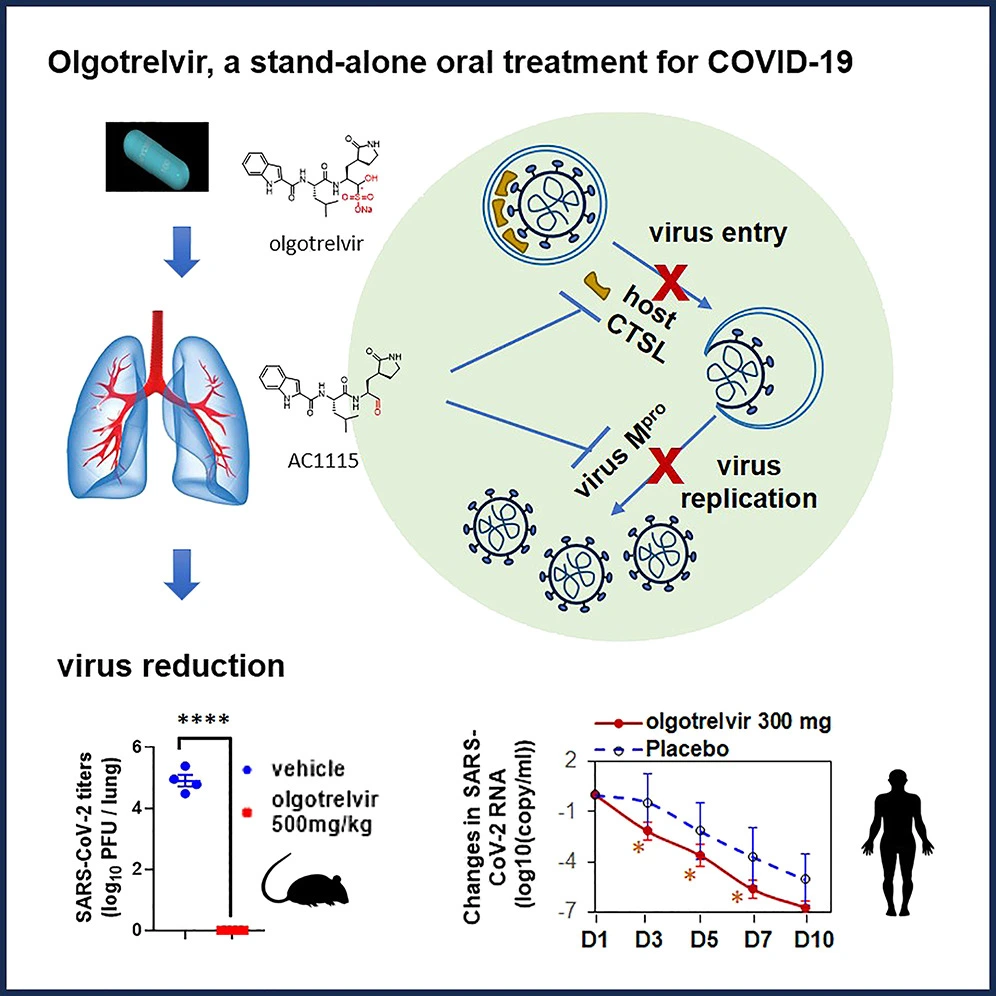
La inhibición de la proteasa principal bloquea la replicación viral, mientras que la inhibición de la catepsina L impide la invasión viral de las células huésped, lo que potencia significativamente su eficacia mediante este doble enfoque.
El Olgotrelvir Sodium es el primer inhibidor de doble acción del mundo que inhibe tanto la proteasa 3CL como la catepsina L, bloqueando así la invasión viral de las células e inhibiendo la replicación viral. Este diseño de doble acción proporciona una respuesta más completa y eficaz contra el nuevo coronavirus en comparación con los fármacos de acción única.
Los datos clínicos de fase III encabezan las listas de las revistas internacionales más prestigiosas
En mayo de 2024, se publicaron los resultados del ensayo clínico de fase III de Olgotrelvir Sodium en NEJM Evidence, una revista subsidiaria del New England Journal of Medicine. Esto proporciona respaldo científico para la aplicación clínica de los fármacos.
El fármaco redujo significativamente el tiempo de recuperación de los pacientes con COVID-19 leve a moderado (tiempo medio de recuperación de 8,56 días, frente a 2,44 días en el grupo placebo) y disminuyó rápidamente la carga viral.
Su eficacia fue especialmente notable en los adultos mayores y en los grupos de alto riesgo de desarrollar una enfermedad grave.
La monoterapia ofrece importantes ventajas en materia de seguridad
A diferencia de los fármacos tradicionales contra la COVID-19, que requieren terapia combinada con ritonavir, el Olgotrelvir Sodium puede administrarse por vía oral como monoterapia, evitando así el riesgo de interacciones medicamentosas asociadas a los inhibidores de las enzimas metabólicas hepáticas.
Los ensayos clínicos de fase I demostraron su alta biodisponibilidad oral y su buena tolerancia tanto en voluntarios sanos como en pacientes. Elimina las preocupaciones sobre interacciones medicamentosas, lo que resulta en un perfil de seguridad más elevado, y es especialmente adecuado para pacientes ancianos y aquellos con afecciones médicas subyacentes.
La innovación China beneficia a pacientes de todo el mundo
El Olgotrelvir Sodium, el primer fármaco innovador de Clase 1 de China para la COVID-19, ha sido sometido a cuatro años de investigación y desarrollo, recibiendo apoyo especial de la Administración Nacional de Productos Médicos (NMPA) mediante una «orientación integral y un respaldo completo».
La Administración Nacional de Productos Médicos (NMPA) ha exigido a las empresas que completen estudios posteriores a la comercialización condicionales dentro de un período específico, y los mayoristas están obligados a cooperar con los requisitos reglamentarios para garantizar el cumplimiento de la distribución de medicamentos.
Xu Wanhong, gerente general de la compañía, declaró que el costo de producción del fármaco es más de un 60% menor que el de los medicamentos importados, y se espera que entre en producción en enero de 2026, con un primer lote destinado tanto al mercado nacional como al internacional.
La aprobación de octavevir llena un vacío en el mercado para el tratamiento de infecciones leves a moderadas por COVID-19, especialmente por su capacidad de simplificar los regímenes de tratamiento al no requerir el uso de ritonavir, lo que se espera que impulse una mayor demanda clínica.
No somos solo un distribuidor farmacéutico; también conectamos y creamos valor a través de medicamentos innovadores. Hong Kong DengYuePharma seguirá manteniéndolo al día con la información farmacéutica más reciente.

FAQ About Olgotrelvir Sodium:
Este fármaco logra un bloqueo dual al inhibir simultáneamente tanto la proteasa principal del coronavirus (Mpro) como la catepsina L (CTSL): el inhibidor de la proteasa principal impide la replicación viral, mientras que el inhibidor de la catepsina L bloquea la invasión viral de las células huésped.
Se utiliza para el tratamiento de la infección leve a moderada por COVID-19 en adultos y se está ampliando al campo de la enfermedad pulmonar obstructiva crónica (EPOC).
Según la información disponible, los datos sobre los efectos secundarios del octavevir sódico provienen principalmente de su ensayo clínico de fase III.
En dicho ensayo, de los 607 pacientes del grupo de tratamiento, el 31 % experimentó eventos adversos de grado 1-2, con una tasa de eventos adversos graves de tan solo el 0,5 %, y no se observaron reacciones adversas graves relacionadas con el fármaco.
1.Personas con alergias: Quienes sean alérgicos al oseltamivir sódico o a cualquier componente del medicamento no deben usarlo para evitar reacciones alérgicas como erupciones cutáneas y dificultad para respirar.
2.Personas con condiciones fisiológicas especiales:
1)Mujeres embarazadas o en período de lactancia: Su uso debe realizarse bajo la supervisión de un médico, tras evaluar los beneficios y los riesgos, para evitar posibles riesgos para el feto o el lactante.
2)Niños y ancianos: Debido a sus capacidades físicas especiales, los ajustes de dosis y la monitorización de las reacciones adversas deben seguirse estrictamente según las indicaciones del médico.
3.Pacientes con enfermedades graves:
1)Pacientes con insuficiencia hepática o renal grave: El metabolismo del medicamento puede verse restringido, lo que puede provocar acumulación y toxicidad. Se deben realizar ajustes de dosis o tratamientos alternativos según las indicaciones del médico.
2)Pacientes con trastornos neurológicos como la miastenia gravis: Medicamentos similares (como el oseltamivir) pueden empeorar los síntomas; se requiere una evaluación cuidadosa.

