En el ámbito del tratamiento del mieloma múltiple (MM), el BCMA (antígeno de maduración de células B) se ha convertido en uno de los objetivos de precisión más representativos. Entre ellos, la terapia CAR-T dirigida a BCMA, gracias a su potente capacidad de eliminación y su efecto de remisión duradera, se considera actualmente una de las modalidades terapéuticas más disruptivas.
A medida que la tecnología continúa evolucionando, el CAR-T contra BCMA está pasando de ser una “terapia innovadora” a convertirse en una “opción estándar de tratamiento”, y está remodelando profundamente el panorama terapéutico de las neoplasias hematológicas.
En el contexto de la aceleración global de la innovación farmacéutica, Dengyue Pharma, apoyándose en una visión global y capacidades profesionales, se dedica a integrar recursos de medicamentos innovadores internacionales y sistemas de cadena de suministro conformes, con el fin de ofrecer a los pacientes vías eficientes y fiables para acceder a terapias innovadoras.
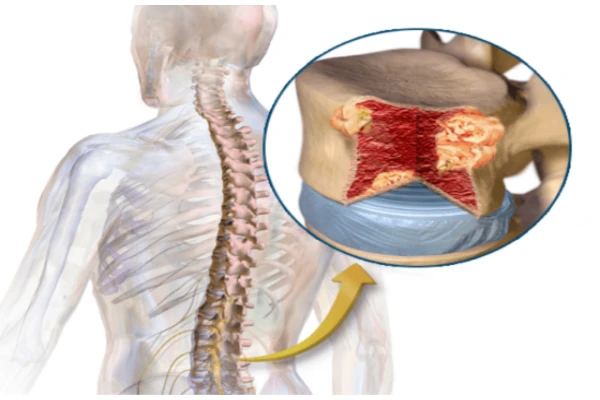
I. Mecanismo central de la terapia CAR-T dirigida a BCMA
El principio fundamental de la tratamiento CAR-T anti-BCMA radica en modificar mediante ingeniería genética las células T autólogas del paciente, para que expresen receptores quiméricos de antígeno (CAR) capaces de reconocer el BCMA, logrando así la identificación y eliminación precisa de las células del mieloma.
El proceso terapéutico incluye:
- Recolección de células T: aislamiento de células T autólogas del paciente
- Modificación genética: introducción del gen que codifica el CAR específico para BCMA
- Expansión in vitro: aumento del número de células CAR-T
- Quimioterapia de acondicionamiento: generalmente ciclofosfamida + fludarabina para depleción linfocitaria
- Reinfusión: las células CAR-T se expanden en el organismo y ejercen efectos antitumorales
La estructura del CAR generalmente incluye:
- Dominio de reconocimiento antigénico scFv
- Región bisagra y estructura transmembrana
- Dominio coestimulador (como CD28, 4-1BB, OX40)
- Dominio de señalización CD3ζ
Este “sistema de reconocimiento inmunitario diseñado” confiere a las CAR-T una altísima especificidad y eficacia citotóxica.
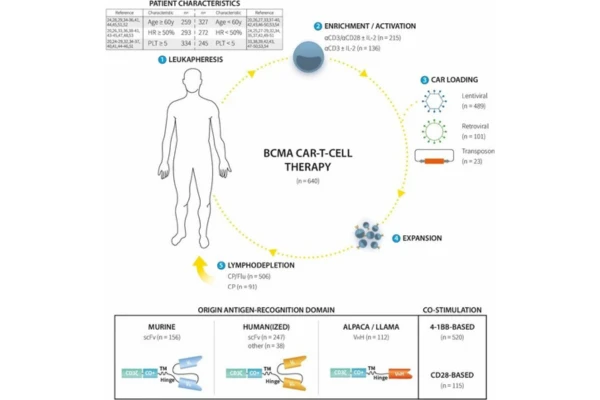
II. Innovaciones clínicas y avances tecnológicos de la terapia CAR-T dirigida a BCMA
Con la profundización de la investigación, la tecnología CAR-T dirigida a BCMA está experimentando innovaciones en múltiples dimensiones:
1️⃣ Nuevas estructuras de reconocimiento antigénico
Las CAR-T de nueva generación optimizan continuamente sus dominios de reconocimiento:
- Estructura VHH totalmente humana (reduce inmunogenicidad)
- Andamiaje Centyrin (mejora estabilidad)
- Diseño de dominio D (incrementa significativamente la tasa de respuesta)
- Estructura trimérica APRIL (permite doble diana BCMA/TACI)
Estos diseños mejoran la capacidad de reconocimiento y reducen el riesgo de escape antigénico.
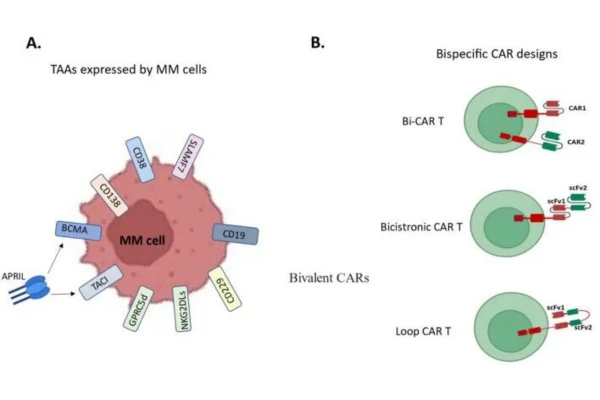
2️⃣ CAR-T de doble diana: nueva tendencia
Para abordar la disminución o pérdida de expresión de BCMA:
- BCMA/CD19
- BCMA/CD38
- BCMA/GPRC5D
Datos clínicos muestran:
- ORR de hasta el 100% en algunos pacientes de alto riesgo
- Aumento significativo de la tasa de negatividad MRD
La estrategia de doble diana se está consolidando como clave para superar la resistencia.
3️⃣ Innovación en plataformas de fabricación
Las nuevas tecnologías están reduciendo drásticamente los tiempos de producción:
- Plataforma rápida T-Charge: 2 días
- Tecnología FasTCAR: 24 horas
- Transfección no viral (piggyBac): reducción de costes
Además, las CAR-T alogénicas (“listas para usar”) avanzan rápidamente:
- Sin necesidad de personalización
- Mayor accesibilidad
Actualmente, la terapia CAR-T dirigida a BCMA mejora continuamente su eficacia y accesibilidad mediante diseño de doble diana y fabricación rápida.
III. Ventajas clave: ¿por qué CAR-T es superior a otras terapias dirigidas a BCMA?
En comparación con los ADC (conjugados anticuerpo-fármaco) o los anticuerpos biespecíficos (BsAb), la terapia CAR-T dirigida a BCMA presenta ventajas significativas:
| Dimensión | Terapia celular CAR-T dirigida a BCMA | ADC (conjugados anticuerpo-fármaco) | Anticuerpos biespecíficos (BsAb) |
|---|---|---|---|
| Capacidad de eliminación | Expansión in vivo con “efecto amplificador”, potencia citotóxica muy alta | Depende de la carga del fármaco, capacidad limitada | Depende de la actividad de las células T |
| Profundidad de respuesta | Mayor tasa de CR/sCR y negatividad de MRD | Algunos pacientes logran respuesta profunda | Puede alcanzar tasas de respuesta relativamente altas |
| Duración del efecto | Puede generar memoria inmunitaria, remisiones duraderas | Requiere administración repetida | Requiere tratamiento continuo |
| Interferencia del objetivo (sBCMA) | Alta tolerancia al “efecto señuelo” | Fácilmente afectado por sBCMA | Impacto moderado |
| Forma de administración | Generalmente una sola infusión | Administración periódica | Administración frecuente o infusión continua |
| Adherencia del paciente | Tratamiento único, alta adherencia | Requiere múltiples ciclos | Alta carga por tratamiento prolongado |
| Velocidad de inicio | Requiere expansión in vivo antes de actuar | Inicio relativamente rápido | Inicio más rápido |
| Accesibilidad | Producción compleja y coste elevado | Relativamente accesible | Ventaja de “listo para usar” |
La terapia CAR-T dirigida a BCMA presenta ventajas claras en capacidad de eliminación, profundidad de respuesta y duración del efecto, siendo actualmente la vía tecnológica más prometedora dentro de las terapias dirigidas a BCMA. Sin embargo, aún requiere mejoras en accesibilidad y costes. Por otro lado, los ADC y los anticuerpos biespecíficos ofrecen valor complementario en términos de disponibilidad inmediata y conveniencia, formando conjuntamente un panorama terapéutico complementario.
IV. Desafíos clave que enfrenta la terapia CAR-T dirigida a BCMA
1. Toxicidad
- Síndrome de liberación de citocinas (CRS)
- Neurotoxicidad (ICANS)
- Riesgo de tumores secundarios
2. Desafíos de eficacia
- Escape antigénico
- Microambiente tumoral inmunosupresor
- Agotamiento de células T
3. Producción y acceso
- Ciclo largo de fabricación
- Alto coste
- Riesgo de rechazo en CAR-T alogénico
Estos factores indican que la tecnología sigue en optimización continua.
V. Optimización tecnológica y futuro
1. Mejora en fabricación
- Producción en 24h–2 días
- Estandarización
- Expansión de CAR-T “off-the-shelf”
2. Diseño de próxima generación
- Multidiana (BCMA + GPRC5D)
- Inhibidores de γ-secretasa
- Modulación de checkpoints
3. Seguridad
- Interruptor iCasp9
- Sistema EGFR truncado
4. Terapias combinadas
- CAR-T + inhibidores del proteasoma
- CAR-T + IMiD
- CAR-T + BsAb o ADC
5. Expansión de indicaciones
- Primera línea en MM de alto riesgo
- Sustitución de ASCT
- Otras enfermedades de células B
6. Exploración avanzada
- CAR-NK derivados de iPSC
- CAR-T in vivo
- CAR-T con edición genética
👉 Estas innovaciones mejorarán la eficacia y reducirán costes.
VI. Conclusión: la terapia CAR-T dirigida a BCMA lidera una nueva era de la medicina de precisión
La terapia CAR-T dirigida a BCMA ha impulsado el tratamiento del mieloma múltiple desde el “control multirlínea” hacia una “remisión profunda e incluso curación funcional”. Su valor no solo reside en la eficacia, sino en redefinir el modelo terapéutico hacia la inmunoterapia de ingeniería.
Con la optimización continua, se espera que:
- Se convierta en tratamiento estándar o de primera línea
- Mejore la supervivencia a largo plazo
- Impulse la era de la terapia celular a gran escala
En el contexto del rápido desarrollo de la medicina de precisión y la ingeniería inmunitaria, la tratamiento CAR-T anti-BCMA no es solo una terapia dirigida, sino un pilar fundamental del futuro tratamiento oncológico.
Basándose en la vanguardia farmacéutica internacional, Hong Kong Dengyue Pharma, con profesionalismo, cumplimiento e innovación como motores clave, construye un puente confiable entre terapias innovadoras globales y las necesidades de los pacientes.
FAQ About terapia CAR-T dirigida a BCMA
Es una forma avanzada de inmunoterapia que modifica genéticamente las células T del paciente para que reconozcan y destruyan células tumorales que expresan el antígeno BCMA, comúnmente presente en el mieloma múltiple.
Se utiliza principalmente para tratar el mieloma múltiple, especialmente en pacientes en recaída o refractarios que no responden a tratamientos convencionales.
Las células T del paciente se extraen, se modifican en laboratorio para expresar un receptor CAR específico contra BCMA, se expanden y luego se reinfunden para atacar directamente las células cancerosas.
Ofrece una alta tasa de respuesta, remisiones profundas (incluyendo negatividad MRD) y efectos duraderos gracias a la memoria inmunitaria.

