En la oncología moderna, comprender el mecanismo de acción de los fármacos ADC se ha convertido en un aspecto fundamental para optimizar la terapia dirigida contra el cáncer. Los conjugados anticuerpo-fármaco (ADC) actúan mediante la entrega selectiva de agentes citotóxicos a las células tumorales, combinando precisión biológica con nuevas capacidades de inmunomodulación tumoral.
La optimización del diseño molecular en los ADC de nueva generación ha permitido superar el modelo tradicional basado únicamente en la liberación intracelular de toxinas, introduciendo mecanismos innovadores como la liberación extracelular de la carga útil y la modulación del microambiente inmunitario tumoral, factores que contribuyen a mejorar la eficacia clínica y ampliar las indicaciones terapéuticas.
Este avance mecanístico está ampliando tanto la eficacia clínica como los límites de las indicaciones terapéuticas de los ADC. En paralelo al rápido desarrollo global de fármacos oncológicos innovadores, los sistemas centrados en la accesibilidad a los medicamentos y la integración de información profesional también están ganando importancia. En este ecosistema, algunas plataformas de servicios farmacéuticos como Hong Kong Dengyue Pharma desempeñan un papel de apoyo relevante.
¿Cómo funciona el mecanismo de acción de los fármacos ADC?
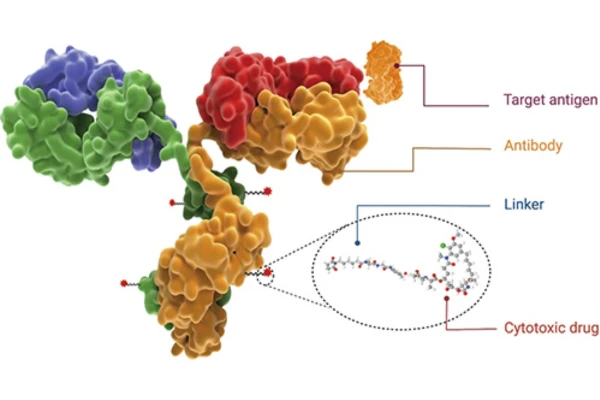
En las investigaciones iniciales y en la práctica clínica temprana, la lógica terapéutica central de los ADC se basaba principalmente en la entrega precisa de cargas citotóxicas. Los ADC suelen estar compuestos por tres elementos fundamentales: un anticuerpo monoclonal, un enlazador (linker) y un fármaco citotóxico de alta potencia. Mediante el reconocimiento de antígenos específicos en la superficie de las células tumorales, el anticuerpo permite la unión selectiva y la posterior internalización del conjugado.
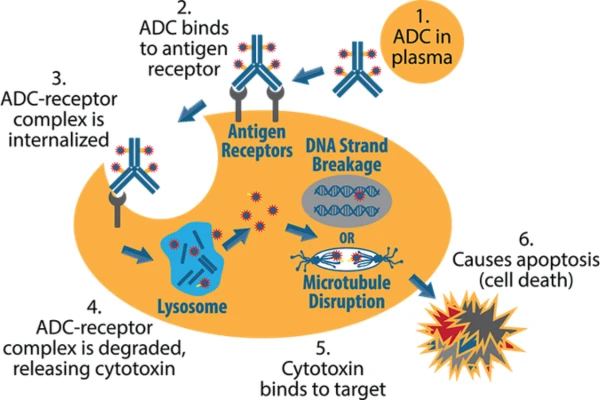
🧪 Una vez dentro de la célula tumoral, el enlazador es escindido por enzimas lisosomales o en condiciones ácidas, liberando la carga citotóxica y provocando efectos como daño en el ADN, alteración de los microtúbulos o detención del ciclo celular. Este mecanismo de acción de los fármacos ADC mejora significativamente la selectividad terapéutica de la quimioterapia y reduce la toxicidad sistémica, representando un avance importante en el tratamiento del cáncer.
⚠️ Sin embargo, con la profundización de la experiencia clínica, se ha reconocido que depender exclusivamente del modelo de administración intracelular presenta limitaciones, como la heterogeneidad en la expresión antigénica tumoral que puede generar respuestas terapéuticas desiguales, así como la presencia de un microambiente inmunosupresor que restringe la profundidad del efecto terapéutico. Estas limitaciones han impulsado la evolución del diseño conceptual de los ADC de nueva generación.
Nuevo mecanismo de acción de los fármacos ADC: liberación extracelular de la carga útil
En los últimos años, los ADC innovadores han logrado avances significativos en la estabilidad de los enlazadores y en las propiedades fisicoquímicas de las cargas útiles, permitiendo que ciertos fármacos se liberen directamente en el microambiente tumoral. Este cambio en el mecanismo de acción de los medicamentos ADC amplía la cobertura antitumoral.
💡 Cuando el ADC libera moléculas citotóxicas en el espacio intercelular tumoral o en la superficie de las células cancerosas, estas pequeñas moléculas pueden difundirse pasivamente hacia células tumorales vecinas, generando el denominado efecto espectador (bystander effect).
Este fenómeno presenta varias ventajas potenciales:
● Permite eliminar células tumorales con baja o nula expresión antigénica
● Aumenta la profundidad terapéutica global en tumores sólidos altamente heterogéneos
● Puede retrasar la expansión selectiva de clones resistentes
Desde la perspectiva de la estrategia terapéutica, la liberación extracelular de la carga útil permite que el mecanismo de acción de los fármacos ADC evolucione desde una dependencia estricta de la expresión antigénica hacia un modelo de tratamiento dirigido al “territorio tumoral”, aumentando así el potencial global de eficacia.
Papel de la inmunomodulación en el mecanismo de acción de los fármacos ADC
Además del efecto citotóxico directo, un número creciente de estudios indica que el mecanismo de acción de los medicamentos ADC también puede influir en el microambiente inmunitario tumoral a través de múltiples vías. Algunas cargas útiles pueden inducir muerte celular inmunogénica (ICD), favoreciendo la liberación de antígenos tumorales y mejorando la capacidad de presentación antigénica de las células dendríticas.
Este proceso puede promover aún más la infiltración de linfocitos T efectores y generar un circuito de retroalimentación inmunitaria positiva, ampliando el impacto terapéutico de los ADC desde la destrucción local de células tumorales hacia la activación de respuestas inmunitarias sistémicas.
🛡️ Además, los ADC pueden contribuir a reducir la actividad de células inmunosupresoras asociadas al tumor, como las células T reguladoras o las células supresoras derivadas de mieloides, facilitando la transición del microambiente tumoral desde un estado “inmunológicamente frío” hacia uno “caliente”. Este efecto inmunomodulador proporciona una base teórica importante para la combinación de ADC con inhibidores de puntos de control inmunitario.
Mecanismo sinérgico: desde la entrega precisa hacia una estrategia antitumoral multidimensional
Cuando la liberación extracelular de la carga útil y los efectos inmunomoduladores actúan de manera coordinada, los ADC de nueva generación pueden influir en múltiples etapas de la progresión tumoral, formando así un efecto antitumoral más profundo y amplio.
🌐 A diferencia del modelo terapéutico tradicional que dependía principalmente de la liberación intracelular de toxinas, este enfoque enfatiza la mejora simultánea de la cobertura espacial dentro del tejido tumoral y la participación del sistema inmunitario. Por ejemplo, por un lado, las cargas citotóxicas liberadas extracelularmente pueden difundirse hacia células tumorales vecinas y generar un efecto espectador significativo, ampliando el alcance del daño directo y mejorando la eficacia frente a tumores con expresión antigénica heterogénea; por otro lado, ciertas cargas útiles pueden inducir muerte celular inmunogénica, promoviendo la liberación de antígenos tumorales, mejorando la presentación antigénica y activando la infiltración de linfocitos T efectores, lo que contribuye a una respuesta inmunitaria sostenida.
⚖️ En este proceso, la acción citotóxica directa y la inmunomodulación suelen mostrar una relación de refuerzo mutuo. La reducción de la carga tumoral puede aliviar el estado inmunosupresor, mientras que la vigilancia inmunitaria continua ayuda a eliminar células tumorales residuales, prolongando la duración de la respuesta terapéutica y reduciendo el riesgo de recaída.

✨ Este modelo de “doble impulso mecanístico” está transformando gradualmente a los ADC de simples herramientas farmacológicas en estrategias terapéuticas integrales con características de plataforma, impulsando además que la investigación clínica preste mayor atención al equilibrio entre profundidad de respuesta, duración del beneficio terapéutico y supervivencia a largo plazo.
Perspectivas clínicas y direcciones de investigación
Con el avance continuo de la ingeniería molecular y la investigación inmunológica, los ADC de nueva generación están explorando estrategias de diseño más innovadoras. Entre ellas, el desarrollo de enlazadores escindibles con mayor estabilidad y características de liberación más controlables podría garantizar la liberación eficaz de la carga útil en el sitio tumoral al tiempo que reduce la toxicidad sistémica. Asimismo, la optimización de la relación fármaco-anticuerpo (DAR) y la mejora del diseño estructural de los anticuerpos pueden potenciar las propiedades farmacocinéticas de estos fármacos y ampliar su ventana terapéutica.
En cuanto a la selección de cargas útiles, los investigadores están intentando introducir nuevas moléculas citotóxicas o moduladores de señal con potencial inmunorregulador, con el objetivo de fortalecer la sinergia entre el mecanismo de acción de los fármacos ADC y las terapias inmunológicas. Esta estrategia no solo podría aumentar la tasa de respuesta objetiva, sino también prolongar la supervivencia libre de progresión y la supervivencia global.
Al mismo tiempo, las estrategias de tratamiento combinado con ADC se están convirtiendo en una dirección clave de investigación clínica. Los modelos de combinación más frecuentes incluyen:
● Combinación con inhibidores de puntos de control inmunitario: para potenciar la liberación de antígenos y la activación de linfocitos T
● Combinación con terapias antiangiogénicas: para mejorar la estructura vascular tumoral y favorecer la penetración del fármaco
● Combinación con terapias dirigidas o quimioterapia convencional: para intervenir múltiples vías de señalización y aumentar la profundidad terapéutica global
A medida que las tecnologías de selección de biomarcadores continúan perfeccionándose, una estratificación más precisa de los pacientes contribuirá a optimizar la aplicación clínica de los ADC, impulsar el desarrollo de terapias personalizadas y ampliar su valor clínico tanto en tumores sólidos como en neoplasias hematológicas.
Resumen
En general, el mecanismo de acción de los fármacos ADC está experimentando una evolución significativa, pasando del modelo tradicional basado en la entrega intracelular precisa hacia un enfoque antitumoral multidimensional impulsado por la difusión extracelular de la carga útil y la inmunomodulación sinérgica. Este avance mecanístico no solo mejora la profundidad del tratamiento, sino que también ofrece nuevas soluciones para superar la heterogeneidad tumoral y la tolerancia inmunológica.
En este proceso, distintos actores de la cadena de valor farmacéutica —incluidas plataformas profesionales de servicios de medicamentos como Hong Kong Dengyue Pharma— contribuirán conjuntamente a la evolución de los modelos terapéuticos. En el futuro, con el perfeccionamiento continuo de la ingeniería molecular, la investigación inmunológica y las estrategias de tratamiento combinado, los ADC están destinados a desempeñar un papel cada vez más central en los sistemas de oncología de precisión, impulsando la terapia contra el cáncer hacia una era más eficiente y personalizada.

FAQ About mecanismo de acción de los fármacos ADC
El mecanismo de acción de los ADC consiste en la unión selectiva del anticuerpo a antígenos tumorales, seguida de la liberación de una carga citotóxica que destruye las células cancerosas.
¿Por qué el mecanismo de acción de los fármacos ADC es más preciso que la quimioterapia tradicional?
Es un fenómeno en el que la carga citotóxica liberada puede difundirse a células tumorales cercanas, ampliando el efecto antitumoral incluso en tumores heterogéneos.
Sí. Algunos ADC pueden inducir muerte celular inmunogénica y favorecer la activación de linfocitos T, potenciando la respuesta inmunitaria contra el tumor.

